5.血糖、乳酸
血糖(Glu)升高是重癥患者常見的病理現象。多年來,諸多的基礎和臨床研究得到幾乎一致的認識,就是高血糖是危重患者的獨立死亡危險因素之一。
乳酸(Lac)是體內糖代謝的中間產物。在某些病理情況下(如呼吸衰竭或循環衰竭時),可引起組織缺氧,由于缺氧可引起體內乳酸升高。
診療方案中的描述:重癥患者組織氧合指標乳酸進行性升高;
常用儀器:生化分析儀、(重癥可使用)血氣分析儀
全自動化程度:不能批量上樣,手動放置樣本
樣本及用量:靜脈血漿、動脈全血
實驗室開展要求:中心檢驗室、重癥監護室
開展難度:★★★☆☆(有難度)
人們可以通過合理或嚴格血糖控制,顯著降低多種疾病并發癥的發生率和病死率。
另外,人體內葡萄糖代謝過程中,如糖酵解速度增加,劇烈運動、脫水時,也可引起體內乳酸升高。體內乳酸升高可引起乳酸中毒。檢查血乳酸水平,可提示潛在疾病的嚴重程度。
新冠肺炎患者臨床研究數據:《柳葉刀》線上1月29日發表的99例患者研究中[7],血糖平均7.4mmol/L(正常參考區間3.9-6.1 mmol/L),51例(52%)患者血糖升高,僅1例患者血糖降低。
6.降鈣素原
降鈣素原(PCT)是全身性細菌感染及膿毒癥的診斷標志物,并可用于輔助鑒別細菌感染和病毒感染。
診療方案中的描述:多數患者降鈣素原正常;
常用儀器:化學發光分析儀
全自動化程度:高、批量進樣
樣本及用量:靜脈血清/血漿
實驗室開展要求:中心檢驗室、急診檢驗室
開展難度:★★☆☆☆(較容易)
當人體受到細菌感染時,細菌被免疫細胞分解所產生的脂多糖會刺激機體產生白介素、腫瘤壞死因子等細胞因子,繼而促進體內脂肪細胞大量分泌PCT;當人體受到病毒感染時,機體受到病毒刺激產生干擾素(INF-γ),而INF-γ的產生則會抑制PCT的生成。可以利用細菌感染后降鈣素原(PCT)升高的特點,將一部分細菌性肺炎患者早期鑒別出來進行對癥治療。
新冠肺炎患者臨床研究數據:《柳葉刀》于1月24日發表的對41例患者研究[6]中,多數患者入院時血清降鈣素原水平正常,四名ICU患者發生繼發感染,其中三名降鈣素原大于0.5ng/ml。《柳葉刀》線上1月29日發表的99例患者研究[7]中,其中4例(4%)膿毒性休克;6例患者(6%)降鈣素原高于正常范圍。
三、病情惡化指標應警惕指標
除前述根據病情應監測的項目外,還有以下指標變化應警惕病情變化:
1.細胞因子
細胞因子(Cytokine, Ck)由免疫細胞(如單核、巨噬細胞、T細胞、B細胞、NK細胞等)和某些非免疫細胞(內皮細胞、表皮細胞、纖維母細胞等)經刺激而合成、分泌的一類具有廣泛生物學活性的小分子蛋白質。
診療方案中的描述:重型、危重型患者常有炎癥因子升高;有條件者可行細胞因子檢測;
常用儀器:流式細胞儀
全自動化程度:低,操作復雜
樣本:血清
實驗室開展要求:免疫學實驗室(尚未在臨床診斷上廣泛開展,多為科研實驗)
開展難度:★★★★☆(較難)
細胞因子一般通過結合相應受體調節細胞生長、分化和效應,調控免疫應答。
細胞因子可被分為白細胞介素(如IL-2、IL-3、IL-4、IL-5、IL-6、IL-9、IL-10、IL-12、IL-13、IL-14等)、干擾素(如IFN-γ)、腫瘤壞死因子超家族(如TNF-β)、集落刺激因子(如GM-CSF)、趨化因子、生長因子等。細胞因子的檢測是基礎免疫研究的有效手段,在臨床疾病診斷、病程觀察、療效判斷及細胞因子治療監測方面有重要價值。
新冠肺炎患者臨床研究數據:《柳葉刀》于1月24日發表的對41例患者研究[6]中,對比了NCP(新冠肺炎)患者中的ICU患者(n=13),非ICU患者(n=28),以及健康人(n=4)的細胞因子濃度,各類細胞因子在ICU組升高明顯高于非ICU組,并且都高于健康對照組。
2.白細胞介素-6
白介素6(IL-6)是一種細胞因子,在人體急性炎癥反應鏈中處于中心地位,誘導產生CRP和PCT等多種主要炎癥因子。
診療方案中的描述:重型、危重型患者常有炎癥因子升高;有條件者可行細胞因子檢測。對于雙肺廣泛病變者及重型患者,且實驗室檢測IL-6水平升高者,可試用托珠單抗治療。
常用儀器:化學發光分析儀
全自動化程度:高
樣本:血清
實驗室開展要求:中心檢驗室
開展難度:★★☆☆☆(較容易)
由于IL-6在炎癥介質網絡中的重要作用,血液中的IL-6濃度水平在多種臨床疾病的病理過程早期均會出現明顯升高,這些疾病主要包括細菌感染、新生兒敗血癥、膿毒血癥、呼吸系統衰竭等。在多種細胞因子中臨床意義最顯著,可用常規方法在臨床廣泛開展。
新冠肺炎患者臨床研究數據:《柳葉刀》1月29日發表的99例患者研究[7]中,有超過半數(52%)的患者IL-6升高。一些重癥的患者體內產生了嚴重的細胞因子風暴,其中體內IL-6甚至達到了413.6pg/mL[8]。
3.淋巴細胞亞群
外周血淋巴細胞根據生物學功能和細胞表面抗原表達分為3個群:T淋巴細胞(CD3+)、B淋巴細胞(CD19+)和NK淋巴細胞。
診療方案中的描述:以下指標變化應警惕病情變化:外周血淋巴細胞計數進行性降低;淋巴細胞中B淋巴細胞明顯降低,CD4及CD8 T細胞不斷下降;
常用儀器:流式細胞儀
全自動化程度:低,操作復雜
樣本:靜脈全血
實驗室開展要求:免疫學實驗室(尚未在臨床診斷上廣泛開展,多為科研實驗)
開展難度:★★★★☆(較難)
T細胞表面可表達多種分化抗原(CD)分子,如CD45、CD3、CD4、CD8、CD5等,這些膜分子對T細胞的檢測、T細胞對抗原的特異性識別和應答,以及T細胞與其他免疫細胞之間的相互作用等都有著不同的生物學作用。T細胞參與細胞免疫反應,B細胞參與體液免疫反應。
淋巴細胞亞群分析是檢測細胞免疫和體液免疫功能的重要指標,其總體反應機體當前的免疫功能、狀態和平衡水平,并可輔助診斷某些免疫缺陷性疾病、變態反應性疾病,分析發病機制,觀察療效及監測預后。
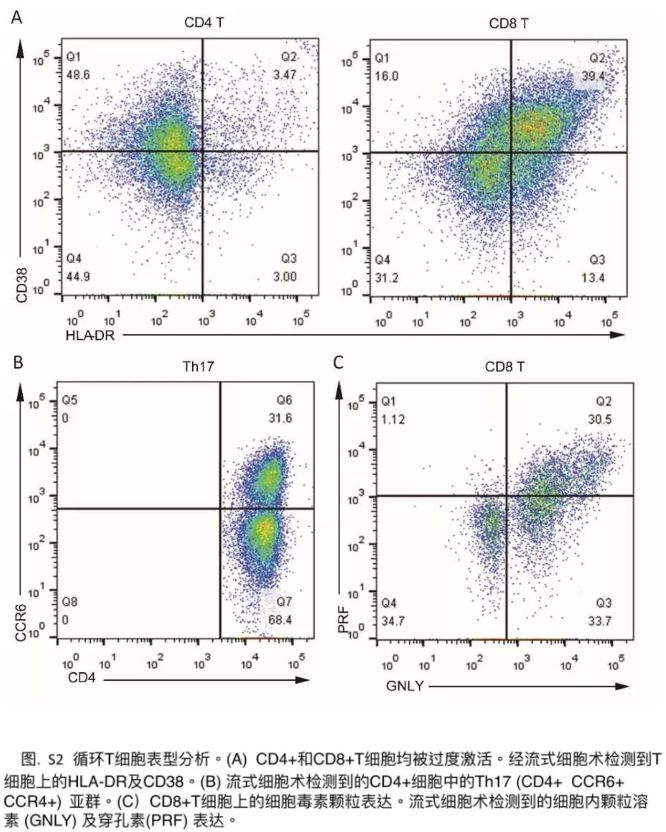
新冠肺炎患者臨床研究數據:《柳葉刀》2月17日發表首例對新冠肺炎死亡患者病理解剖的分析報告[9]中,外周血流式細胞術分析發現,外周血CD4+和CD8+細胞的數量大大減少,而它們的狀態卻被過度激活。CD4+T細胞中具有高度促炎效應的CCR4+ CCR6+ Th17細胞增加。此外,發現 CD8+T細胞有高濃度的細胞毒性顆粒,其中31.6%的細胞為穿孔素陽性,64.2%細胞為顆粒溶素陽性,30.5%細胞為顆粒溶素和穿孔素雙陽性(附錄p3)。我們的結果表明,以Th17的增加和CD8+T細胞的高細胞毒性為表現的T細胞過度活化,能夠部分地解釋該患者的嚴重免疫損傷。
四、臨床確診指標
1.病毒核酸檢測
所有生物除朊病毒外都含有核酸,核酸包括脫氧核糖核酸(DNA)和核糖核酸(RNA),新型冠狀病毒是一種RNA病毒,通過鑒定病毒中的保守RNA序列可以將其與其他病原體進行區分。
診療方案中的描述:病原學確診證據之一:采用RT-PCR或/和NGS方法在鼻咽拭子、痰和其他下呼吸遞分泌物、血液、糞便等標本中可檢測出新型冠狀病毒核酸。檢測下呼吸道標本(痰或氣道抽取物)更加準確。標本采集后盡快送檢。
常用儀器:核酸檢測分析系統
全自動化程度:低,操作復雜、步驟多、耗時長
樣本:咽拭子、痰液、呼吸道分泌物
檢測時間:1個工作日
實驗室開展要求:核酸檢測實驗室
開展難度:★★★★☆(較難)
檢測新型冠狀病毒特異序列的方法最常見的是熒光定量PCR(聚合酶鏈式反應)。因PCR反應模板僅為DNA,因此在進行PCR反應前,應將新型冠狀病毒核酸(RNA)逆轉錄為DNA。在PCR反應體系中,包含一對特異性引物以及一個Taqman探針,該探針為一段特異性寡核苷酸序列,兩端分別標記了報告熒光基團和淬滅熒光基團。探針完整時,報告基團發射的熒光信號被淬滅基團吸收;如反應體系存在靶序列,PCR反應時探針與模板結合,DNA聚合酶沿模板利用酶的外切酶活性將探針酶切降解,報告基團與淬滅基團分離,發出熒光。每擴增一條DNA鏈,就有一個熒光分子產生。
熒光定量PCR儀能夠監測出熒光到達預先設定閾值的循環數(Ct值)與病毒核酸濃度有關,病毒核酸濃度越高,Ct值越小。不同生產企業的產品會依據自身產品的性能確定本產品的陽性判斷值。
新冠肺炎患者臨床研究數據:中國醫學科學院院長王辰院士2月5日接受央視采訪時曾表示,“這個病有個特點,并不是所有患病者都能檢測出核酸陽性。對于真是這個病的病人,也不過只有30%-50%的陽性率。”
2.病毒基因測序
病原宏基因組測序(mNGS)是目前臨床上針對病原最常用的基因測序方法,是一種基于二代測序技術的無需培養、無偏好性的病原檢測技術,可一次性完成細菌、真菌、病毒和寄生蟲等多種病原體檢測。
診療方案中的描述:病原學確診證據之一:病毒基因測序,與已知的新型冠狀病毒高度同源;
常用儀器:測序儀
全自動化程度:低,需先進行核酸提取
樣本:血液、痰液、肺泡灌洗液、組織液、拭子等
檢測時間:1周內
實驗室開展要求:臨床基因擴增實驗室
開展難度:★★★★★(高難度)
此次疫情中,病原宏基因組測序 (mNGS)利用其技術優勢,在五天內就鑒定并分析出新型冠狀病毒的基因組,而2003年SARS的鑒定耗時5月余、2013年H7N9的鑒定耗時1月余。因此,病原宏基因組測序 (mNGS)為本次疫情感染病原體的進一步確認以及防控爭取了時間,也為后續的臨床診斷、治療和藥物研發指明了方向[10]。
新冠肺炎患者臨床研究數據:2020年1月10日,上海市公共衛生臨床中心和公共衛生學院與華中科技大學武漢市中心醫院、武漢市疾病預防控制中心、國家傳染病預防控制所、中國疾病預防控制中心和澳大利亞悉尼大學合作,公開了2019冠狀病毒基因組。
經數據分析,2019-nCoV與2003年爆發的SARS病毒基因組序列相似度為80%,與2017年2月從國內的蝙蝠中采集到的Bat SARS-like coronavirus isolate bat-SL-CoVZC45基因組序列相似性最高,相似度為88%。對2019-nCoV病毒株的基因組變異分析為追溯病毒來源、追蹤病毒株變異路徑、防控新型冠狀病毒引發的疫情、治療病毒性肺炎提供重要的數據基礎與決策支持。
3.病毒抗體檢測
IgM、IgG是機體對于病毒免疫應答的關鍵組成部分,臨床上血清IgM、IgG抗體檢測是病毒感染非常必要的、常規的實驗室檢查手段,比如乙肝病毒、丙肝病毒等,都是通過檢測病毒刺激機體后產生的血清抗體來輔助診斷。
診療方案中的描述:血清學檢查:新型冠狀病毒特異性IgM抗體多在發病3-5天后開始出現陽性,IgG抗體滴度恢復期較急性期有4倍及以上增高。血清學確診證據:
常用儀器:無需儀器,或免疫分析儀
全自動化程度:低
樣本:靜脈全血、血清
檢測時間:操作簡便,15分鐘可完成檢測
實驗室開展要求:一般門診檢驗室
開展難度:★☆☆☆☆(非常容易)
一般來說,最早產生的抗體是IgM,在機體受病原刺激一周左右出現,IgM持續時間較短。而后產生IgM的B細胞進入淋巴結,在生發中心接受輔助性T細胞和抗原提呈細胞的刺激,進一步成熟分化為漿細胞,大量產生IgG,IgG持續時間較長。因此,往往IgM抗體陽性表示近期感染,IgG抗體陽性表示感染時間較長或既往感染。
針對新冠病毒的特異性抗體檢測,可用膠體金或化學發光法測病毒IgM及IgG,可在患者感染第7天或發病第3天就檢測出來,對于進一步的確診會很有幫助。
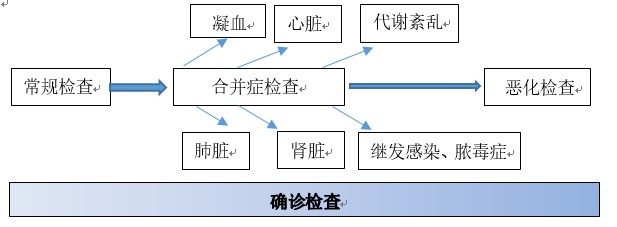
通過這些檢測指標的分類介紹,是否更好的了解每項檢查的意義了呢?從這些指標也可以看出患者初期就診首先進行常規檢查,結合合并并發癥的相關檢查、臨床癥狀和其他輔助檢測(如CT)手段及流行病學調查等,可以進行初步診斷;然后對疑似患者進行確診檢查;對危重癥患者動態監測,觀察病情變化。
【參考文獻】
1. 《新型冠狀病毒肺炎診療方案(試行第七版)》
2. 《新型冠狀病毒肺炎重型、危重型病例診療方案(試行第二版)》
3. Guan W, Ni Z, Hu Y, et al. Clinical characteristics of 2019 novel coronavirus infection china. MedRxiv preprint, 2020,2,6.
4. Wang D, Hu B, Hu C, et al. Clinical Characteristics of 138 Hospitalized Patients With 2019 Novel Coronavirus–Infected Pneumonia in Wuhan, China. JAMA, Online February 7, 2020.
5. 新型冠狀病毒肺炎相關靜脈血栓栓塞癥防治建議(試行). 中華醫學雜志, 2020,100(00) : E007-E007.
6. Huang C, Wang Y, Li X,et al. Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China. Lancet. 2020 Jan 24.
7. Chen N, Zhou M, Dong X, et al.Epidemiological and clinical characteristics of 99 cases of 2019 novel coronavirus pneumonia in Wuhan, China: a descriptive study. Lancet 2020, 395: 507–13.
8. Fang Y, Zhang H, Xu Y, et al. CT Manifestations of Two Cases of 2019 Novel Coronavirus(2019-nCoV) Pneumonia. 2020 Feb 7.
9. Xu Z, Shi L, Wang Y, et al. Pathological findings of COVID-19 associated with acute respiratory distress syndrome. Lancet. 2020 Feb 17.
10. 陶悅、傅啟華、莫茜等. 病原宏基因組測序在新型冠狀病毒檢測中的應用與挑戰. 中華檢驗醫學雜志, 2020,43:網絡預發表.